Силы на поверхности
Инженер Н. Садиленко
Из крана течет вода. Закручивайте кран — струйка становится тоньше, еще
тоньше и вдруг... разбивается на капли. Никакими силами нельзя сделать, чтобы
струйка стала тонкой, как паутинка. Почему?
 Мыльный
пузырь имеет форму шара. Почему не форму пресс-папье или сороконожки? Мыльный
пузырь имеет форму шара. Почему не форму пресс-папье или сороконожки?
Почему уголь в противогазе поглощает разные отравляющие газы: и хлор, и
фосген, и другие? В чем здесь секрет?
Непослушание струйки, форма мыльного пузыря, секрет угля объясняются силами,
возникающими на поверхности веществ, поверхностными явлениями.
Посмотрите на цветную вкладку. Поверхностные явления встречаются и в природе
и в технике. Люди научились использовать их, заставили служить себе. Чистая
водопроводная вода, непромокаемый плащ, с которого вода скатывается, как с гуся,
флотация (один из методов обогащения полезных ископаемых), смазка машин имеют
самое непосредственное отношение к поверхностным явлениям. Вы можете проделать
интересные опыты, позволяющие понять сущность поверхностных явлений и сил,
которые их вызывают.
Говорят, что жидкость имеет форму сосуда, в который она налита. В самом деле,
если, например, воду поместить в бутылку, то она примет форму бутылки.
Молекулы жидкости не так прочно связаны друг с другом, как молекулы твердого
тела. Силы притяжения к Земле не могут изменить форму лежащего на столе мелового
брусочка. А брусочек воды на стол не положишь. Сила тяжести перемещает молекулы
воды и разливает ее по столу.
- Какую же форму имеет жидкость в действительности? Чтобы ответить на
вопрос, нужно увидеть ее в свободном состоянии, без искажающего ее форму
влияния силы тяжести. Бельгийский физик Плато придумал опыт, который вы
можете легко повторить (см. цветную вкладку). Нальем в широкую банку соленую
воду (3 0/0 соли). Затем
возьмем стаканчик с анилином (можно взять подсолнечное масло и смесь воды со
спиртом), закроем картонкой, погрузим в воду и выпустим его содержимое. Вы
увидите, что действительно естественная форма жидкости — шар. Ведь анилин со
всех сторон окружен соленой водой, имеющей одинаковую с ним плотность, и
находится в воде во взвешенном состоянии.
- Если анилиновый шар проткнуть палочкой и вращать ее сначала медленно, а
затем ускоряя, то в конце концов от него начнут отрываться отдельные капли.
По инерции они будут вращаться вокруг центрального шара, как планеты вокруг
Солнца.
- В несоленой воде анилин тонет, но при нагревании он становится легче
воды и всплывает, вернее начинает капать вверх большими красивыми каплями
(опыт Дарлинга).
- Естественную форму принимает жидкость и при падении с большой высоты.
Этим пользуются, чтобы делать круглую дробь. В высокой дробелитейной башне
заставляют расплавленный металл капать. Капли, пролетев Огромный путь,
принимают форму шариков и даже успевают остыть. Чтобы они не расплющились,
подставляют чан с водой.
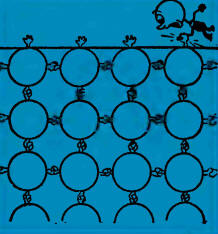
- Молекулы жидкости связаны силами сцепления: они как бы держат друг друга
за руки (см. рис.). У молекул, которые находятся на поверхности, остаются
как бы свободные руки.
Поверхностные молекулы как бы натягивают поверхность жидкости, делают ее
прочной, упругой. Вот и создается впечатление, что на поверхности имеется
прочная пленка.
- Если иглу смазать жиром, то она, казалось бы вопреки силам природы, —
ведь сталь почти в восемь раз тяжелее воды, — будет плавать как обыкновенная
деревянная щепка.
- Вот еще один старый, но эффектный опыт. Если в маленький стаканчик, до
краев наполненный водой, осторожно опустить булавку, то вода не прольется.
Попробуйте опустить еще одну булавку, еще десять, двадцать. Что за чудо? Вы
опустили уже тысячу булавок, вода приподнялась над стаканом, ее поверхность
выгнулась, но ни одной капли не скатилось на стол. Поверхностное натяжение
удерживает воду в стакане.
- Поверхностное натяжение определяет форму мыльного пузыря. Мыльная пленка
пытается сжаться, сделаться меньше, а самую меньшую поверхность оболочка
мыльного пузыря будет иметь только тогда, когда пузырь примет форму шара.
- Мыльные пузыри помогают гасить огонь.
В огнетушителе имеется сода и соляная кислота. При ударе штифтом о что-нибудь
твердое внутри огнетушителя разбивается ампула, кислота смешивается с содой,
образуется углекислый газ. Он горения не поддерживает. Молекулы его занимают
место вокруг пламени, отгоняя молекулы нужного для горения кислорода, и огонь
гаснет. А если будет Ветер? Он, попросту говоря, сдует углекислый газ и доставит
к очагу пожара свежий кислород. Как же погасить огонь на ветру? Для этого в
огнетушитель наряду с содой и кислотой помещают порошок лакричного корня. Этот
порошок, как мыло, образует с водой пузырьки с прочными пленками. Теперь из
огнетушителя выходит струя пены, каждый пузырек которой наполнен углекислым
газом. В пузырьках пены углекислый газ защищен от ветра, и такой пеной легче
гасить огонь на ветру или на вертикальной стене, к которой пена может прилипать.
Сейчас химики искусственно делают хорошие вспениватели. Сливая растворы соды
и соляной кислоты с добавкой вспенивателя и без него, можно проверить роль такой
добавки.
Если химического вспенивателя у вас нет, можно взять в аптеке мыльный корень
и прокипятить его в воде. Полученная при этом вытяжка будет неплохим
вспенивателем.
Почему капельки воды не могут в виде шариков кататься по полу, как ртуть?
Почему вода разливается? Дело в том, что притяжение между частицами ртути
сильнее, чем притяжение частиц ртути к частицам деревянного пола. Говорят, что
ртуть не смачивает дерево, а вода его смачивает: ее частицы притягиваются к
частицам дерева сильнее, чем друг к другу.
Если опустить тонкую стеклянную трубку в ртуть, то уровень ртути в трубке
будет ниже, чем вне ее. А если опустить трубку в воду, то уровень воды в трубке
повысится. По таким тонким капиллярным трубочкам, превозмогая силу тяжести,
тянется вверх вода в травинке и глинистом обрыве берега, тянется вверх по фитилю
спирт в спиртовке и керосин в лампе. А посмотрите, какая интересная форма
поверхности в капилляре! У ртути — выпуклая, а у воды — вогнутая (см. рис.).
- Можно сделать забавный опыт «Русские горы» (см. вкладку). Вода не
смачивает сажу и капли-шарики стремительно несутся вниз.
- Поверхностные силы могут удержать воду даже в решете. Нужно только
сделать так, чтобы вода не смачивала его. Окунем решето с мелкой сеткой в
расплавленный парафин и быстро вынем. Проволочки решета покрылись тонким
слоем парафина, который водой не смачивается. Отверстия уменьшились, но
остались. Теперь осторожно зачерпнем решетом воду — молекулы воды стремятся
быть вместе, сторонятся парафина и не проливаются сквозь решето. Если
внимательно посмотреть, то даже видно, что вода несколько провисает в
ячейках решета.
- Если молекулы газов соприкасаются с поверхностью воды, то «свободные
руки» поверхностных молекул сейчас же хватают их и удерживают. Это явление
называется адсорбцией. Поверхностные силы проявляются не только на
поверхности жидкости, но и у твердого тела. Чем больше поверхность тела, тем
сильнее ее действие. Очень большую поверхность можно получить, измельчая
тело в порошок или поони-зывая его трещинками. Сумма поверхности всех
пылинок огромна. Поэтому у небольшой горстки пыли большой запас
поверхностной энергии. Древесный уголь имеет неровную поверхность и весь
пронизан мельчайшими трещинками: он тоже обладает большой энергией.
- Уголь, помещенный в противогаз, спас миллионы человеческих жизней в
период первой мировой войны, защитив их от отравляющих газов. Древесный
уголь благодаря адсорбции всегда имеет на своей поверхности притянутые
молекулы газов воздуха и паров воды. Его поры забиты смолистыми веществами.
Если такой уголек прокалить, то посторонние молекулы покидают его. Уголь, из
которого удалены адсорбированные газы и смолистые вещества, называют
активированным.
 Кусочек активированного угля может поглотить аммиака больше
своего собственного объема в 180 раз, а отравляющего газа фосгена — даже в
440 раз. Где же помещается в угольке столько газа? На внешней поверхности
уголька и в трещинках. Адсорбированные молекулы газов очень тесно покрывают
эту поверхность. Сейчас в противогазах, как ив заводских аппаратах, кроме
угля, применяют и другие «жадные вещества» — адсорбенты, например силикатель
и алюмогель, а также бентонитовые глины. Кусочек активированного угля может поглотить аммиака больше
своего собственного объема в 180 раз, а отравляющего газа фосгена — даже в
440 раз. Где же помещается в угольке столько газа? На внешней поверхности
уголька и в трещинках. Адсорбированные молекулы газов очень тесно покрывают
эту поверхность. Сейчас в противогазах, как ив заводских аппаратах, кроме
угля, применяют и другие «жадные вещества» — адсорбенты, например силикатель
и алюмогель, а также бентонитовые глины.
- Тресковый суп вкусен, но запах его не для всех приятен. Поверхностные
силы вам помогут. Возьмите кусочек древесного угля, накалите его и бросьте в
суп. Уголек адсорбирует частички, создающие запах.
- Адсорбцию также используют для очистки воды в водопроводах, пропуская
воду сквозь песок. Огромная общая поверхность песчинок адсорбирует всякие
примеси, и из песка выходит очень чистая вода.
- Было замечено, что одни вещества адсорбируются легче, другие — труднее.
В адсорбционной колонке — трубке со слоями адсорбентов — можно разделять
смеси веществ, например нефтепродуктов.
- По различию окраски слоев адсорбентов узнают даже, какие вещества
имеются в смеси. Такой анализ называют хроматографическим. Для него иногда
вместо адсорбентов просто применяют фильтровальную бумагу. По капиллярам бумаги одни вещества
продвинутся дальше, другие ближе, и по этим цветным пятнам можно узнать, какие
вещества были в смеси.
Иногда адсорбция приносит и вред. С нее начинается ржавление. Поверхность
металла адсорбирует молекулы кислорода, воды. Этим молекулы как будто хотят сами
побыстрее покрыть металлическую поверхность, поверхностные молекулы железа
притягивают их своими избыточными силами. Сначала происходит адсорбция, а после
этого адсорбированные молекулы начинают атаку против частиц поверхностного слоя
металла; они «выковыривают» такие частицы, соединяясь с ними. Появляется
ржавчина (см. рис.).
Заканчивая наш короткий рассказ о силах на поверхности, хочется пожелать,
чтобы вы продолжили путешествие в мир этих удивительных явлений, проделав опыты.
|
|